mikroskop elektronowy Służy do obserwacji ultrastruktury materii: komórek, tkanek czy kryształów. Zamiast światła widzialnego używana jest wiązka elektronów, wytwarzana przez działo elektronowe. Ultracienkie skrawki preparatów (20-60 nm) umieszczane są na mosiężnych siatkach, będących odpowiednikami szklanych płytek w mikroskopach świetlnych. Preparaty muszą być utrwalone i naprószone solami metali ciężkich (osmu, ołowiu, uranu etc. ). Atomy tych metali powodują odchylenie trasy elektronów, dzięki czemu powstaje kontrastowy obraz preparatu, obserwowany na ekranie ektroluminescencyjnym, a w nowszych urządzeniach za pomocą matryc CCD. Pierwszy mikroskop elektronowy zbudowali w 1931 r. niemieccy fizycy Ernst Ruska i Maks Knoll z Wyższej Szkoły Technicznej w Berlinie (od 1946r. Uniwersytet Techniczny). Był to mikroskop transmisyjny. Instrument wdrożyła do produkcji firma Siemens (1938 r.), jednak zastosowanie w laboratoriach badawczych datuje się po II wojnie światowej (w Polsce od lat 1960-tych). Rozwój mikroskopów elektronowych polega na zmniejszaniu rozmiarów oprzyrządowania, zwiększaniu przyspieszenia elektronów (poprzez poprawę wydajności działka i akceleratorów oraz pomp próżniowych) czy wprowadzaniu nowych technik mikroskopowych: mikroskopy skaningowe, refleksyjne, emisyjne. W Krakowie działały jedne z pierwszych mikroskopów w kraju (po Warszawie i Gliwicach). Japońskie JEM 5Y zostały zakupione w 1963 r. dla Akademii Górniczo-Hutniczej i Instytutu Zoologii UJ. Decyzją ówczesnego rektora UJ Zygmunta Grodzińskiego (kadencja 1956-62) zakup mikroskopu dla UJ został sfinansowany z pieniędzy z zapisu testamentowego Ignacego Jana Paderewskiego.
Mikroskop elektronowy transmisyjny (TEM)
Wyposażenie mikroskopu stanowi zasilacz wysokiego napięcia (Tesla BS 2420) oraz zasilacz stabilizowany prądu stałego 24 V (Tesla BP 2420).
Instrument zakupiony w drugiej połowie lat 1960-tych do Instytutu Zoologii UJ dla Zakładu Zoologii Systematycznej i Zoogeografii (od 2011 r. Zakład Biologii Rozwoju i Morfologii Bezkręgowców). Przekazany następnie do Instytutu Fizyki, skąd trafił do Muzeum.
fot. Grzegorz Zygier
Fragment tkanki przeznaczony do oglądania w mikroskopie elektronowym musi być zabezpieczony przed deformacją. Stosuje się najpierw dwuetapowy proces utrwalania: najpierw związek o pH zbliżonym do tkanki, zabezpieczający przed jej odwodnieniem, następnie czterotlenek osmu, mający równocześnie właściwości kontrastujące.
Zdjęcia z mikroskopu GEM 5Y
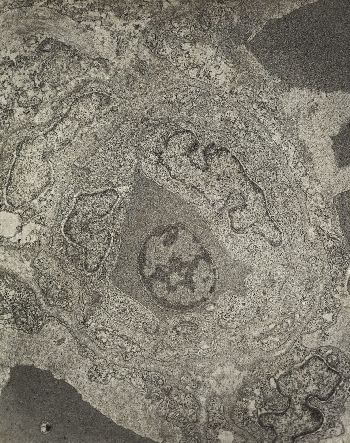

Zdjecie po lewej przedstawia fragment kapilary gruczołu gazowego okonia. Lata 1960-1970te.
Widoczny wzór ciemnych punktów, tworzących wzór organelli powstaje w wyniku naprószenia powierzchni solami metali ciężkich. W innym wypadku kontrast poszczególnych elementów byłby zbyt mały dla otrzymania rysunku.
Zdjęcie po prawej przedstawia izolowane DNA ssaków metodą Klein-Schmidta. Ciemne punkty powstają przez ugięcie drogi elektronów na atomach matali ciężkich naprószonych na preparat w procesie kontrastowania. Lata 1960-1970-te (?))
Zdjęcia są własnością Muzeum Zoologicznego UJ
Zdjęcia wykonane na mikroskopie GEM 5Y w ówczesnym Zakładzie Anatomii Porównawczej, przygotowano na wystawę propagującą mikroskop elektronowy jako nowy instrument laboratoryjny. Autorami wystawy byli profesorzy Andrzej Jasiński i Wincenty M. Kilarski. Wykorzystane zostały również w albumie ich autorstwa Ultrastruktura komórki (Warszawa, 1984r.).
Butla po EPON 812

Jest to butla po głównym składniku żywicy epoksydowej, w której zalewa się preparat.
Butla przekazana do Muzeum przez Zakład Biologii i Obrazowania Komórki UJ
fot. Grzegorz Zygier
Kolejnym etapem jest stopniowe odwadnianie, analogiczne do mikroskopii tradycyjnej. Przygotowanie do cięcia na skrawki o grubości 20 - 60 nm polega na zatopieniu w trójskładnikowej żywicy epoksydowej: głównym składnikiem jest Epon 812, mieszany z dwoma dodatkowymi składnikami i katalizatorem przyspieszającym polimeryzację (utwardzanie) żywicy. Obecnie stosuje się również poręczniejsze żywice akrylowe.
Tkanki umieszcza się w specjalnych gumowych foremkach lub żelatynowych kapsułkach, gdzie po zatopieniu w żywicy formowane są bloczki. Z bloczków usuwa się nadmiar żywicy na szlifierkach, formując stożki.
Obrabiarka uniwersalna

Nadmiar bardzo twardej żywicy epoksydowej usuwa się na szlifierce, dzięki czemu bloczek ma kształt stożka, w którego szczycie tkanka otoczona jest niewielką ilością żywicy.
Instrument przekazany przez Zakład Biologii i Obrazowania Komórki UJ
fot. Grzegorz Zygier
Po pierwszym pocięciu na skrawki, oglądane są one pod mikroskopem świetlnym w celu wybrania fragmentu przeznaczonego do dalszych badań. Otrzymane skrawki tkanki można wybarwić tkanki (błękit metylenowy, błękit toluidynowy, azur II), szczególnie w przypadku żywic akrylowych. Jednak najważniejsze jest jej skontrastowanie, czyli "barwienie" solami metali ciężkich, zwykle octanem uranylu czy cytrynianem ołowiu. Atomy metali ciężkich: osmu, ołowiu uranu itd. powodują zakrzywienie toru elektronów i uwydatnienie struktur komórkowych
Noże diamentowe do ultramikrotomu

Produkowane z diamentów technicznych co wiąże się z ceną jaką trzeba za nie zapłacić. W efekcie używane są do cięcia wybranych skrawków, w innych przypadkach stosowane są noże szklane.
Noże przekazane przez Zakład Biologii i Obrazowania Komórki UJ
fot. Grzegorz Zygier
Ze względu na cenę noży diamentowych powszechnie używa się ich zamienników - noży szklanych. Cięte są ze specjalnych pasków szklanych szk ła o wysokiej jakości. Wykrawanie ostrza następuje albo na specjalnych urządzeniach, albo przy użyciu diamentowego rysika i specjalnych kleszczy do łamania tafli. Początkowo wycina się kwadraty, dzielone potem wzdłuż przekątnej na trójkąty. Jakość krawędzi tnącej kontroluje się pod lupą stereoskopową. Do wyselekcjonowanych noży szklanych montuje się wanienki z tworzywa sztucznego lub folii metalowej i uszczelnia płynną parafiną lub szybkoschnącym lakierem
ła o wysokiej jakości. Wykrawanie ostrza następuje albo na specjalnych urządzeniach, albo przy użyciu diamentowego rysika i specjalnych kleszczy do łamania tafli. Początkowo wycina się kwadraty, dzielone potem wzdłuż przekątnej na trójkąty. Jakość krawędzi tnącej kontroluje się pod lupą stereoskopową. Do wyselekcjonowanych noży szklanych montuje się wanienki z tworzywa sztucznego lub folii metalowej i uszczelnia płynną parafiną lub szybkoschnącym lakierem
Kleszcze do łamania noży szklanych i uzyskane noże
Kleszcze należały do prof. Wincentego Kilarskiego.
Kleszcze przekazane przez Zakład Biologii i Obrazowania Komórki UJ
fot. Grzegorz Zygier
Ultramikrotom automatyczny
 Urządzenie do skrawania tkanki z dużą precyzją.
Urządzenie do skrawania tkanki z dużą precyzją.
Instrument przekazany przez Zakład Biologii i Obrazowania Komórki UJ
fot. Grzegorz Zygier
Po wybarwieniu, skrawki przenosi się na siatki miedziane, będące odpowiednikiem szkiełka podstawowego w mikroskopach świetlnych. Przeniesienie skrawków na siatkę odbywa się poprzez dotknięcie siatką powierzchni skrawków pływających w wanience noża mikrotomowego. Po skontrastowaniu solami metali ciężkich, zwykle osmu, ołowiu czy uranu, nadają się do oglądania w mikroskopie. Siatki mosiężne od lat 1970-tych produkowane są fabrycznie, wcześniej wykrawane były z siatki specjalnymi wycinakami.
Urządzenie do wykrawania siatek podstawowych



Początkowo krążki siatki wycinane były z listka siatki miedzianej w laboratoriach. Wprowadzone fabryczne produkty ze wzmocnionym brzegiem ułatwiły pracę. Niekiedy w badaniach immunocytochemicznych czy autoradiograficznych stosuje się siatki niklowe lub złote. Najpopularniejsze i najtańsze są nadal sietki mosieżne.
Przyrząd przekazany przez Zakład Biologii i Obrazowania Komórki UJ
fot. Grzegorz Zygier

